Späte Rübenfäule
Rhizoctone brun (franz.); Rhizoctonia root and crown rot (engl.)
wissenschaftlicher Name: Rhizoctonia solani J.G. Kühn (anamorph), Thanatephorus cucumeris (A.B. Frank) Donk (teleomorph)
Taxonomie: Fungi, Basidiomycota, Agaricomycotina, Agaricomycetes, Cantharellales, Ceratobasidiaceae
Rhizoctonia solani (Anastomosegruppe 2-2) ist der Erreger der späten Rübenfäule. R. solani ist ein bodenbürtiger Krankheitserreger und befällt ausser Zuckerrüben auch Sojabohnen, Ackerbohnen, Mais und verschiedene Gräserarten. Der Pilz verursacht ein nesterweises Absterben der Pflanzen und damit auch Ertragsausfälle. Befallene Rüben haben einen tieferen Zuckergehalt als gesunde Rüben. Die Einhaltung einer mehrjährigen Anbaupause von Zuckerrüben in der Fruchtfolge ist eine wichtige vorbeugende Massnahme. Warme Witterung und hohe Bodenfeuchtigkeit fördern den Befall durch R. solani.

 Abb. 1. Die Späte Rübenfäule wird durch Rhizoctonia solani verursacht, typisch ist ein nesterweises Absterben der Zuckerrübenpflanzen.
Abb. 1. Die Späte Rübenfäule wird durch Rhizoctonia solani verursacht, typisch ist ein nesterweises Absterben der Zuckerrübenpflanzen.
Krankheitsbild
Ab Juli/August beginnen die Rübenblätter nesterweise zu welken (Abb. 1 und 2). Oft sind an der Basis der Blattstiele dunkelbraune Flecken zu erkennen. Die Blätter sterben ab, bleiben aber am Rübenkörper haften und legen sich sternförmig um die Rübe auf den Boden. Diese versucht neue Blätter zu bilden, bevor sie abstirbt.
Unterhalb der Bodenoberfläche findet man am Rübenkörper braun verfärbte, trockene Faulstellen, die häufig von Myzel mit kleinen Sklerotien besetzt sind. Die Faulstellen sind rund bis oval, breiten sich oberflächlich sehr schnell aus, wachsen zusammen oder zeigen ein Muster, das an Sprossen einer Leiter erinnert. Befallene Rüben haben im Endstadium der Krankheit oft tiefe Risse und sind deformiert. Ein Schnitt durch den Rübenkörper zeigt, dass das gesunde Gewebe deutlich vom kranken abgegrenzt ist. Anfänglich ist die Faulstelle auf die äusserste Schicht der Wurzel beschränkt, später dringt sie tief ins Gewebe ein. Die Fäule entwickelt sich von aussen nach innen.
Die Späte Rübenfäule tritt häufig in Fruchtfolgen mit Mais und Ansaatwiesen auf.
Verwechslungsmöglichkeiten
Die Späte Rübenfäule kann leicht mit anderen Fäulen verwechselt werden.
- Die Herz- und Trockenfäule wird durch Bormangel verursacht. Die trockene Fäule beginnt oben in der Mitte des Rübenkörpers.
- Stock- und Stängelälchen (Ditylenchus dipsaci) verursachen eine Fäulnis am Rübenkopf.
- Der Gürtelschorf (Actinobakterien, Aphanomyces cochlioides) verursacht Einschnürungen und wulstartige Wucherungen am Rübenkörper.
Ein sicherer Nachweis von R. solani kann nur im Labor erfolgen (ELISA oder molekular-biologische Methoden). Unter dem Mikroskop erkennt man den Pilz anhand seiner rechtwinkligen Verzweigungen der Hyphen.
Krankheitserreger
Rhizoctonia solani kommt weltweit in nahezu allen Böden vor, wobei die grössten Schäden auf schweren und feuchten Böden auftreten. Der Pilz bildet keine Sporen sondern ein charakteristisches stark verzweigtes Myzel und Sklerotien (Dauerkörper). Die Verzweigungen der Haupthyphen stehen mehr oder weniger rechtwinklig zueinander (Abb. 3). Nach der Verzweigung ist die neue Hyphe zuerst verengt und hat anschliessend eine Querwand (Septum). Die Hyphen sind hell bis dunkelbraun, vielkernig und haben keine Schnallen. Die Sklerotien messen 0.1 - 1 mm im Durchmesser, sind dunkel-braun und bestehen aus einem dichten Geflecht aus fassförmigen Zellen.
Die sexuelle Form (Teleomorphe) Thanatephorus cucumeris wird auf Blattstielen gebildet und besteht aus einer Fruchtschicht mit Basidien, welche Basidiosporen abschnüren.
Von Rhizoctonia solani existieren verschiedene Rassen, die in 13 verschiedene Anastomosegruppen (AG) eingeteilt werden (Tsror 2010, Strausbaugh et al. 2011). Rhizoctonia-Erreger, die eine Hyphenverschmelzung erfolgreich durchführen können, gehören zur derselben Anastomosegruppe (Miedaner et al. 2018). Je nach Zugehörigkeit zu einer AG kann R. solani unterschiedliche Kulturen befallen. Die AG 2-2 ist der Erreger der späten Rübenfäule. Innerhalb dieser AG werden die beiden Untergruppen IIIB und IV unterschieden, die sich durch einen mehr oder weniger engen Wirtspflanzenkreis kennzeichnen. Die AG 2-2 IIIB ist aggressiver und befällt auch Sojabohnen, Bohnen, Mais und verschiedene Gräser. Die AG 2-2 verursacht auch eine Umfallkrankheit an Zuckerrüben-Keimlingen, allerdings ist auf den Keimpflanzen die AG 4 häufiger anzutreffen als AG 2-2.
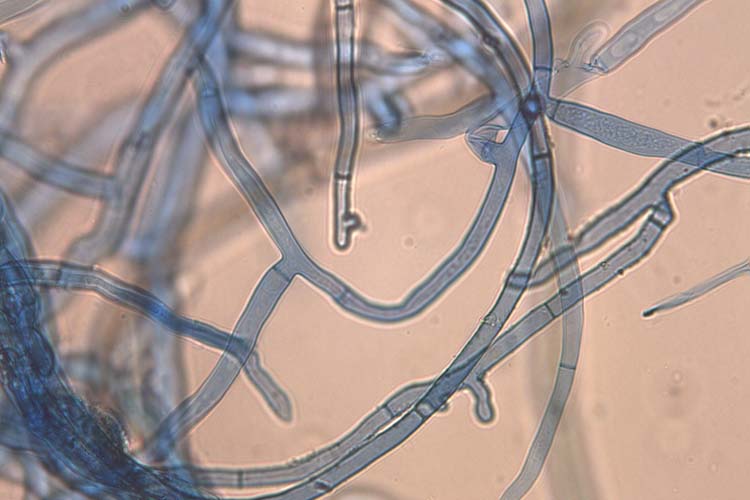 Abb. 3. Myzel von Rhizoctonia solani: Die Verzweigungen der Haupthyphen stehen rechtwinklig zueinander.
Abb. 3. Myzel von Rhizoctonia solani: Die Verzweigungen der Haupthyphen stehen rechtwinklig zueinander.
Lebenszyklus und Epidemiologie
Rhizoctonia solani überdauert als verdickte Hyphe oder in Form von Sklerotien mehrere Jahre im Boden. Der Krankheitserreger kann auch als Saprophyt (als Myzel) auf abgestorbener organischer Substanz überleben. Eine Infektion der Zuckerrüben erfolgt bei Bodentemperaturen zwischen 12 und 35 °C (Harveson et al. 2009). Die Hyphen befallen die Blattstiele, den Rübenkopf und die Wurzel. Sie dringen mit Hilfe von zellwandauflösenden Enzymen direkt in das Pflanzengewebe ein. Werden die Leitbahnen der Pflanze befallen, kann die Wasser- und Nährstoffzufuhr unterbrochen werden, die Pflanze beginnt zu welken und stirbt ab. Gelangt während der Bewirtschaftung infizierter Boden auf den Rübenkopf, kann die Infektion verstärkt werden.
Die Späte Rübenfäule kommt grundsätzlich in allen Böden vor. Eine schlechte Bodenstruktur und eine hohe Bodenfeuchte begünstigen allerdings die Ausbreitung.
Wirtsspektrum
Die Anastomosegruppe AG 2-2 IIIB befällt ausser Zuckerrüben auch Sojabohnen, Ackerbohnen, Mais und verschiedene Gräserarten. Die AG 2-2 IV findet man an Zuckerrüben und verschiedenen Gräserarten. Die AG 2-2 kann die Kartoffel nicht befallen, diese wird vor allem von der AG 3 infiziert. Wirtspflanzen der AG 4 sind Zuckerrüben (Keimlingsbefall), Tomaten, Erbsen, Kartoffeln und Sojabohnen.
Vorbeugende Massnahmen und Bekämpfung
- Fruchtfolge: Eine Anbaupause von mindestens drei Jahren einhalten! Wobei während der Anbaupausen keine Wirtspflanzen der R. solani AG 2-2 angebaut werden sollten. Ein Verzicht auf Mais zugunsten von Getreidearten hat den grössten Effekt auf die Minderung des Schadens der Zuckerrübe (Miedaner et al. 2018). Auch müssen in dieser Zeit Unkräuter konsequent bekämpft werden, da R. solani AG 2-2 zahlreiche Unkrautarten befallen kann: unter anderem den weissen Gänsefuss (Chenopodium album). Infektionen über den Boden können dadurch weitgehend verhindert werden.
- Sortenwahl: Einige Sorten zeigen eine geringere Anfälligkeit. In bekannten Befallsstandorten kann eine gegen R. solani tolerante Sorte angebaut werden.
- Alle Massnahmen, welche ein schnelles Wachstum der Zuckerrüben fördern: Auf eine gute Bodenstruktur achten, Bodenverdichtungen und Staunässe verhindern und auf eine angepasste Kalk- und Humusversorgung achten
- Infizierte Erde sollte bei der Bewirtschaftung der Felder nicht auf den Rübenkopf gelangen.
- Der Einsatz von Antagonisten und Hyperparsiten (Bacillus subtilis, Verticillium biguttatum, Trichoderma harzianum etc.) als biologische Pflanzenschutzmittel können R. solani unterdrücken.
- Tiefwurzelnde Zwischenfrüchte (Ölrettich, Gelbsenf etc.) fördern die Antagonisten und verbessern die Bodenstruktur.
Literatur
Harveson RM, Hanson LE, Hein GL, 2009. Compendium of Beet Diseases and Pests. The American Phytopathological Society, Auflage 2: 140 S.
Miedaner T, Beyer W, Flath K, Hausladen H, Holtschulte B, Kessel B, Koopmann B, Schubiger FX, von Tiedemann A, Zellner M, 2018. Management von Pilzkrankheiten im Ackerbau. Agrimedia, Erling Verlag: 280 S.
Strausbaugh CA, Eujayl IA, Panella LW, Hanson LE, 2011. Virulence, distribution and diversity of Rhizoctonia solani from sugar beet in Idaho and Oregon. Can. J. Plant Pathol. 33 (2): 210-226.
Tsror L, 2010. Biology, Epidemiology and Management of Rhizoctonia solani on Potato. Journal of Phytopathology 158: 649-658.




