Echter Mehltau an Rosen
l'oïdium du rosier (franz.); powdery mildew of rose (engl.)
wissenschaftlicher Name: Podosphaera pannosa (Wallr.) de Bary
Synonyme: Sphaerotheca pannosa (Wallr.) Lév. var. rosae, Erysiphe pannosa (Wallr.) Fries
Taxonomie: Fungi, Ascomycota, Pezizomycotina, Leotiomycetes, Leotiomycetidae, Erysiphales (Helotiales), Erysiphaceae
Der Rosenmehltau (Podosphaera pannosa) ist eine weit verbreitete Pilzkrankheit von Gewächshaus- und Freilandrosen. Er verursacht einen mehlig-weissen Belag an jungen Trieben, Blättern, Knospen und Blüten. Bei Freilandrosen ist mit dem Auftreten des Echten Mehltaus zu rechnen, wenn es wenig oder gar nicht regnet, der Temperaturbereich nahezu optimal ist und die Luftfeuchtigkeit nachts hoch und tagsüber niedrig ist. Sollten diese Bedingungen eintreten, ist der Einsatz von schützenden Fungiziden gerechtfertigt.
 Abb. 1. Rosenmehltau (Podosphaera pannosa)
Abb. 1. Rosenmehltau (Podosphaera pannosa)
Schadbild
Ab Frühling bis in den Herbst sind die jungen Triebe (auch Dornen), Blätter und Knospen mit einem mehlig-weissen Belag bedeckt (Abb. 1 und 2). Der Mehltaupilz kann auch die Blüten befallen und auf den Blütenstielen, Kelchblättern und dem Blütenboden wachsen, besonders wenn die Blütenknospe noch nicht geöffnet ist. Ältere Blätter werden in der Regel nicht infiziert.
Der Belag besteht aus Pilzfäden (Myzel) und Sporen (Konidien). Er wird mit der Zeit dichter und schliesslich filzartig und graubraun. Die Triebe und Blätter sind verdreht, deformiert und oft rötlich angelaufen. Die befallenen Blätter können vorzeitig abfallen.
Im Freien überwintert der Echte Mehltaupilz in Knospen und kann im Frühling neue Triebe infizieren, die sich aus diesen infizierten Knospen entwickeln.
Ein starker Mehltaubefall reduziert das Pflanzenwachstum und mindert auch den ästhetischen Wert der Pflanzen.
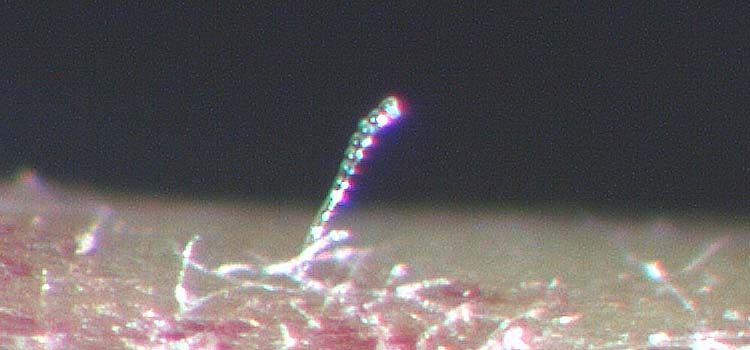
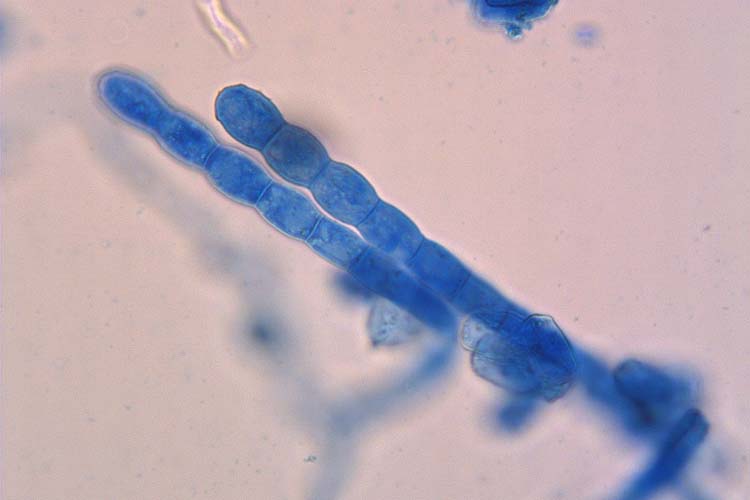 Abb. 3. Die Konidien des Rosenmehltaus (Podosphaera pannosa) wachsen in zusammenhängenden Ketten
Abb. 3. Die Konidien des Rosenmehltaus (Podosphaera pannosa) wachsen in zusammenhängenden Ketten
Krankheitserreger
Der oberflächlich wachsende Mehltaubelag besteht aus septierten Hyphen. An diesen werden auf Konidienträgern ellipsenförmige Konidien gebildet, die in Ketten zusammenhängen (Abb. 3). Die Konidien sind 22.9-28.6 µm lang und 13.6-15.8 µm breit (Horst und Cloyd, 2007).
Die Hauptfruchtform des Mehltaupilzes, ein Kleistothecium, wird nur selten gebildet. Die Kleistothecien sind kugel- bis birnenförmig und haben einen Durchmesser von 85-120 µm, mit einigen kurzen, myzelartigen, septierten Anhängseln. Die Asci sind länglich bis kugelförmig, messen 88-115 µm und enthalten acht Ascosporen, die 12-15 x 20-27 µm gross sind. Neben dem Myzel in ruhenden Knospen, sind Kleistothecien mit den Asci und Ascosporen eine weitere Möglichkeit der Überwinterung des Pilzes.
Innerhalb der Art P. pannosa existieren zahlreiche physiologische Rassen (Linde und Debener, 2003). Jede Rasse befällt nur bestimmte Rosensorten und hat die Fähigkeit bestimmte Resistenzgene zu überwinden. Dies führt bei einer Pflanze, die nur dieses eine Resistenzgen enthält, zu einer Infektion und zur Bildung von Myzel und Konidien. Pflanzen, die andere Resistenzgene enthalten, welche von dieser bestimmten Rasse nicht überwunden werden können (= Mehltaurasse ist avirulent), bleiben gesund. Hier setzt die Pflanzenzüchtung an. Sie versucht möglichst breit wirksame Resistenzgene in einer Rosensorte zu vereinen, um diese gegen möglichst viele Rassen resistent zu machen. Die Resistenzzüchtung erleidet aber immer wieder Rückschläge, da neue Rassen entstehen, die diese Resistenz überwinden können.
Lebenszyklus
An Rosen, die im Freien in Regionen mit strengen Wintern angebaut werden, überwintert der Mehltaupilz als Myzel im Innern von Knospenschuppen. Wenn sich solche Knospen entwickeln, werden die entstehenden Triebe infiziert und es kommt zur Bildung von neuen Konidien (ungeschlechtlich gebildete Pilzsporen). Diese werden über die Luft auf neu entstehende Blätter übertragen, wo sie einen neuen Krankheitszyklus einleiten.
Der Pilz kann auch als Kleistothecium (Hauptfruchtform) überwintern. Allerdings werden diese so unregelmässig gebildet, dass es unwahrscheinlich ist, dass dieser Mechanismus ein effektives Mittel zur Überwinterung darstellt (Horst und Cloyd, 2007).
In milden Klimazonen und in Gewächshäusern sind jederzeit lebensfähige Konidien vorhanden, die neue Infektionszyklen erzeugen können. Der Mehltaupilz ist hier nicht auf eine spezielle Überwinterungsstrategie angewiesen.
Gelangen Konidien des Mehltaupilzes auf eine Wirtspflanze beginnen sie innerhalb 2-4 h zu keimen und bilden Haftorgane (Appressorien) auf den Blättern. Unmittelbar unter dem Appressorium dringt eine Infektionshyphe durch die Kutikula und die Epidermiszellwand ins Innere der Epidermiszelle ein. Hier bildet der Pilz Haustorien, welche ihm zur Nahrungsaufnahme dienen. Auf der Pflanzenoberfläche entwickelt sich ein dicht verzweigtes Geflecht von Myzel, das weitere Haustorien bildet. Am Myzel entstehen Konidienträger mit Konidien, die wiederum Pflanzen befallen können. Eine längere Blattnässedauer hemmt die Entwicklung der Echten Mehltaupilze.
Epidemiologie
Der Rosenmehltau wächst auf jungen Trieben und Blättern besonders gut, während das Pflanzengewebe mit zunehmendem Alter resistenter gegen Infektionen wird. Typischerweise steigt die Mehltauentwicklung, wenn sich neue Triebe entwickeln und nimmt ab, wenn diese Triebe reifen und in Blütenknospen enden. Nach dem Ende der Blüte folgt ein erneuter Anstieg des Mehltaubefalls, wenn die Seitenknospen sich öffnen und sich neue Triebe entwickeln.
Neben der Anfälligkeit des Wirtsgewebes haben auch die Temperatur, die relative Luftfeuchtigkeit und die Anwesenheit von freiem Wasser einen starken Einfluss auf das Wachstum des Rosenmehltaus. Im Freiland sind die günstigsten Bedingungen für den Echten Mehltau wie folgt: Nachts ermöglichen eine Temperatur von 15 °C und eine relative Luftfeuchtigkeit von 90-99 % eine optimale Bildung von Konidien, die Keimung und die Infektion (Horst und Cloyd, 2007). Bedingungen von 26 °C und 40-70 % relativer Luftfeuchtigkeit am Tag begünstigen die Reifung und Freisetzung der Konidien. Mehrere wiederholte Nacht-Tag-Zyklen dieser Bedingungen sind notwendig, damit sich eine Epidemie entwickeln kann.
Das Vorhandensein eines Wasserfilms auf der Blattoberfläche beeinflusst die Entwicklung des Echten Mehltaus negativ. Dieser Effekt ist stark ausgeprägt, wenn die Blätter unmittelbar nach der Ablagerung der Konidien befeuchtet werden. Offenbar keimen die Konidien nicht ohne weiteres in einem Feuchtigkeitsfilm.
Wirtsspektrum
Podosphaera pannosa befällt Rosen und Prunus Arten (Pfirsich, Mandeln und Aprikosen). Isolate des Rosenmehltaus unterscheiden sich morphologisch nicht von Isolaten, die auf Prunus-Arten (wie Pfirsich, Mandel und Aprikose) gefunden werden. Es kann eine gewisse Spezialisierung festgestellt werden, bei der Isolate von Rosen weniger schädlich für Prunus-Arten sind und umgekehrt.
Vorbeugende Massnahmen und direkte Bekämpfung
- Anbau von mehltauresistenten Rosensorten
- Im Frühjahr befallene Triebe möglichst schnell herausschneiden.
- Ende Saison infizierte Triebe zurückschneiden und vernichten, dadurch kann die Überwinterung des Pilzes weitgehend verhindert werden.
- Keine übermässige Stickstoffdüngung
- Für eine gute Durchlüftung des Bestandes sorgen.
- Eine vorbeugende Bekämpfungsmassnahme im Gewächshaus ist das Absenken der Luftfeuchtigkeit in der Nacht durch Ventilatoren, Lüften oder beides oder durch Heizen und Lüften.
- Eine direkte Bekämpfung ist mit Armicarb (Kalium-Bicarbonat) oder Backpulver, Fenicur (ätherisches Öl von Fenchelsamen, vorbeugend) oder Netzschwefel Stulln möglich (siehe auch Andermatt Biocontrol)
- Wirksame, chemisch synthetisch Fungizide stehen im Handel ebenfalls zur Verfügung.
Literatur
Horst RK, Cloyd RA, 2007. Compendium of Rose Diseases and Pests. Second edition. The American Phytopathological Society, 83 p.
Linde M, Debener T, 2003. Isolation and identification of eight races of powdery mildew of roses (Podosphaera pannosa) (Wallr.: Fr.) de Bary and the genetic analysis of the resistance gene Rpp1. Theor Appl Genet 107, 256–262.




